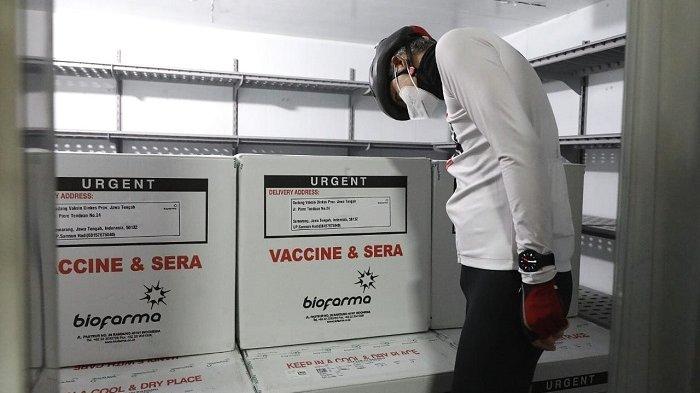
Vaksin Covid19
Sudah Didistribusikan, Vaksin Sinovac Ternyata Belum Dapat Izin dari BPOM dan Sertifikasi MUI
Izin EUA hanya bisa dikeluarkan setelah hasil kajian vaksin telah memenuhi syarat dari aspek keamanan, khasiat dan mutu produk vaksin.
Penulis: Mochammad Dipa | Editor: Feryanto Hadi
WARTAKOTALIVE.COM, JAKARTA - Vaksin Covid-19 dari perusahaan Sinovac telah mulai didistribusikan ke sejumlah daerahdi Indonesia.
Vaksin tersebut rencananya akan diberikan pada kelompok prioritas utamanya para tenaga medis.
Meskipun telah didistribusikan, sejauh ini Badan Pengawas Obat dan Makanan (BPOM) belum
mengeluarkan izin penggunaan darurat atau Emergency Use Authorization (EUA) terkait dengan vaksin
tersebut.
Lalu kenapa perlu adanya izin EUA?
Juru Bicara Vaksinasi Covid-19 dari Badan Pengawas Obat dan Makanan (BPOM) Lucia Rizka Andalusia mengatakan, bahwa saat ini dunia dihadapkan dengan pandemi Covid-19 yang belum ada vaksin dan obatnya.
Baca juga: Sertifikasi Halal Vaksin Covid-19, LPPOM MUI Masih Tunggu Kelengkapan Informasi
Meski demikian, izin EUA hanya bisa dikeluarkan setelah hasil kajian vaksin telah memenuhi syarat dari aspek keamanan, khasiat dan mutu produk vaksin.
“EUA ini bukan hanya Indonesia saja yang punya tapi semua negara punya. Dan tentunya WHO punya
standar EUA untuk pemberian izin dari vaksin khususnya dalam kondisi pandemi Covid-19. Inilah yang
menjadi rujukan BPOM untuk memberikan persetujuan (izin EUA),” ujar Lucia dalam webinar bertajuk
"Kehalalan & Keamanan Vaksin Covid-19," Selasa (5/1/2021).
Rizka menyebut, saat ini BPOM masih menyelesaikan evaluasi terhadap data uji klinis fase 3 vaksin
Sinovac.
Baca juga: Temui KH Maruf Amin, Sandi Diminta Pulihkan Pariwisata dan Ekonomi Kreatif di Berbagai Sektor
Proses ini diperlukan untuk menerbitkan izin EUA. Evaluasi dilakukan terhadap data dukung
keamanan, khasiat dan mutu dari vaksin. Adapun proses evaluasi dilakukan BPOM bersama Komite
Nasional Penilaian Obat serta tim ahli di bidang imunologi dan vaksin yang tergabung dalam Indonesian
Technical Advisory Group on Immunization (Itagi).
"Apabila berdasarkan hasil evaluasi tersebut dinyatakan vaksin Covid-19 memenuhi syarat keamanan,
khasiat dan mutu, serta pertimbangan bahwa kemanfaatan jauh lebih besar daripada risiko, tentunya
(izin EUA) akan dapat diterbitkan," kata Rizka.
Baca juga: Jokowi Akan Tetap Bangun Infrastruktur.di Tahun 2021, Tengku Zulkarnain: Pakai Duit dari Mana?
Persyaratan vaksin disetujui dengan skema EUA
Rizka menjelaskan ada beberapa persyaratan yang harus dipenuhi baik dari aspek keamanan, khasiat
dan mutu, agar vaksin dapat disetujui dengan skema EUA.
Keamanan
Dari aspek keamanan, vaksin ini aman dari subyek penelitian setelah mendapatkan suntikan, serta tidak
menimbulkan efek samping paska pemberian vaksin.
“Keamanan dari subyek penelitian setelah mendapatkan suntikan dipantau terus. Mulai dari 30 menit
setelah suntikan, kemudian 7 hari, 14 hari, 30 hari, 3 bulan sampai 6 bulan terus kita pantau apakah ada
efek samping paska pemberian vaksinasi,” ucapnya.
Baca juga: Disebut Dedengkot Tua oleh Natalius Pigai, AM Hendropriyono: Kamu Bukan Pigai yang Dulu
Khasiat